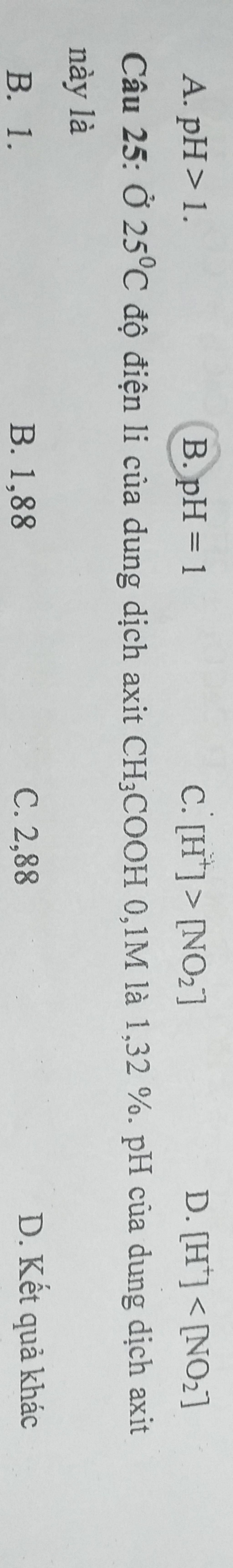Lưu
- Hóa Học
- Lớp 11
- 10 điểm
- thanhthiecdang -
Ở 25°C độ điện li của dung dịch axit CH3COOH 0,1M là 1,32% pH của dung dịch axit này là
Hãy luôn nhớ cảm ơn và vote 5*
nếu câu trả lời hữu ích nhé!
TRẢ LỜI
Đáp án + Giải thích các bước giải:
$-$Gọi $x$ là nồng độ $H_3O^+$ phân li ra.
Theo thuyết $Brønsted:$
$CH_3COOH+H_2O$ $\rightleftharpoons$$CH_3COO^-+H_3O^+$
$x(M)$ ← $x(M)$
$-$Ở $25°C$ độ điện li của dung dịch axit $CH_3COOH$ $0,1(M)$ là $1,32$%
$⇒\dfrac{x}{0,1}$ x $100$%$=1,32$%
$⇒x=1,32$ x $10^{-3}(M)=10^{-2,88}(M)$
$⇒[H^+]=10^{-2,88}⇒pH=2,88$
Hãy giúp mọi người biết câu trả lời này thế nào?
Đăng nhập để hỏi chi tiết
Bạn muốn hỏi điều gì?
A. pH > 1.
B. pH = 1
C. [H] > [NO₂]
D. [H] <[NO₂]
Câu 25: Ở 25°C độ điện li của dung dịch axit CH3COOH 0,1M là 1,32 %. pH của dung dịch axit
này là
B. 1.
D. Kết quả khác
B. 1,88
C. 2,88
Bảng tin
Bạn muốn hỏi điều gì?
 Inbox: m.me/hoidap247online
Inbox: m.me/hoidap247online Trụ sở: Tầng 7, Tòa Intracom, số 82 Dịch Vọng Hậu, Cầu Giấy, Hà Nội.
Trụ sở: Tầng 7, Tòa Intracom, số 82 Dịch Vọng Hậu, Cầu Giấy, Hà Nội.
Giấy phép thiết lập mạng xã hội trên mạng số 331/GP-BTTTT do Bộ Thông tin và Truyền thông.