

có các thí nghiệm sau được tiến hành: TN1: Cho mẩu Na vào nước lỏng dư TN2: Cho mẩu Na như trên vào dd HCl nồng độ 0,1M với thể tích dd HCl bằng thể tích nước ở trên TN3: Cho bột nhôm có số mol = số mol Na trong TN1 vào nước lỏng dư ( thể tích nước = thể tích nước trong TN1) Cho bt hiện tượng xảy ra trong mỗi thí nghiệm và so sánh mức độ phản ứng trong các thí nghiệm
Hãy luôn nhớ cảm ơn và vote 5*
nếu câu trả lời hữu ích nhé!
TRẢ LỜI
Đáp án:
$*)$ Phản ứng xảy ra:
$Na+H_2O\to NaOH+\dfrac 12H_2$
$2Na+2HCl\to 2NaCl + H_2$
$2Al+6H_2O\to 2Al(OH)_3+3H_2$
Hiện tượng xảy ra ở 3 thí nghiệm: đều có sủi bọt khí thoát ra.
Mức độ xảy ra phản ứng: TN3 < TN1 < TN2
Giải thích: - Do dung dịch axit HCl có tính axit mạnh hơn nước $\to$ TN2 > TN1.
- TN3: tạo kết tủa bao bọc Al làm khó phản ứng, hoặc có thể không phản ứng nữa $\to$ Tốc độ giải phóng $H_2$ kém nhất.
Hãy giúp mọi người biết câu trả lời này thế nào?
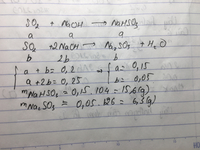
PTHH:
2Na+2H2O=>2NaOH+H2
2Na+2HCI=>2NaCI+H2
2AI+6H2O=>2AI(OH)3+3H2
Nêu được hiện tượng xảy ra ở mỗi trường hợp trên,Đặc biệt:
-Cả 3 TN đều có bọt khí thốt ra
-Mức độ xảy ra phản ứng theo thứ tự:TN2>TN1>TN3
Giải thích:
Do dung dịch HCI có tính axit mạnh hơn nước nên TN2>TN1.TN3 tạo kết của bao bọc AI làm phản ứng khó hoặc không xảy ra nữa nên tốc độ H2 giải phóng kém nhất.
Nhớ cho mk ctl hay nhất nhé
Hãy giúp mọi người biết câu trả lời này thế nào?
Bạn muốn hỏi điều gì?
Bảng tin
Bạn muốn hỏi điều gì?
 Inbox: m.me/hoidap247online
Inbox: m.me/hoidap247online Trụ sở: Tầng 7, Tòa Intracom, số 82 Dịch Vọng Hậu, Cầu Giấy, Hà Nội.
Trụ sở: Tầng 7, Tòa Intracom, số 82 Dịch Vọng Hậu, Cầu Giấy, Hà Nội.










0
5
0
https://hoidap247.com/cau-hoi/488376 Anh ơi giúp e với