

Lưu
- Hóa Học
- Lớp 9
- 20 điểm
- byjuhgbyjuh_13 -
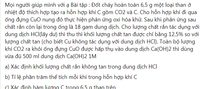
Đốt cháy hết m (gam) một mẫu than (chứa 4% tạp chất trơ, còn lại là cacbon) bởi V(lít) khí Oxi thu được 2,24 lít hỗn hợp chất khí x (dktc). Sục khí X vào dung dịch nước vôi trong dư thấy tạo thành 8 gam kết tủa. Tính giá trị của m và V biết thể tích các khí đều do ở dktc
Hãy luôn nhớ cảm ơn và vote 5*
nếu câu trả lời hữu ích nhé!
TRẢ LỜI
- quangcuong347

Đây là một chuyên gia không còn hoạt động
X gồm O2 dư và CO2
CO2+ Ca(OH)2 -> CaCO3+ H2O
nCaCO3= nCO2= 0,08 mol
nX= 0,1 mol
=> nO2 dư= 0,02 mol
C+ O2 $\buildrel{{t^o}}\over\longrightarrow$ CO2
=> nC= nO2 phản ứng= nCO2= 0,08 mol
Tổng nO2= 0,08+0,02= 0,1 mol
=> V= 2,24l
mC= 0,08.12= 0,96g
Than chứa 96% C nên lượng than đem đốt là 0,96:96%= 1g
Hãy giúp mọi người biết câu trả lời này thế nào?
3.73 vote
Bạn muốn hỏi điều gì?
Bảng tin
Bạn muốn hỏi điều gì?
 Inbox: m.me/hoidap247online
Inbox: m.me/hoidap247online Trụ sở: Tầng 7, Tòa Intracom, số 82 Dịch Vọng Hậu, Cầu Giấy, Hà Nội.
Trụ sở: Tầng 7, Tòa Intracom, số 82 Dịch Vọng Hậu, Cầu Giấy, Hà Nội.
Giấy phép thiết lập mạng xã hội trên mạng số 331/GP-BTTTT do Bộ Thông tin và Truyền thông.








101
2386
62
sai r a Cường ơi
1313
24339
1284
anh ơi em hỏi một chút là làm như thế nào để xét trong hh khí có `O_2 ; CO_2` hoặc là `CO; CO_2`