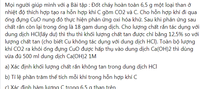
Đốt cháy 2,08 tấn quặng FeS2 và FeS trong đó FeS2 chiếm 57,7% khối lượng để diều chế khí SO2 dùng để sản xuất axit sunfuric H2SO4. Hãy tính thể tích khí O2 ở đktc cần dùng và khối lượng khí SO2 thu được
Hãy luôn nhớ cảm ơn và vote 5*
nếu câu trả lời hữu ích nhé!
TRẢ LỜI
- nhatduong

Đáp án:
VO2 cần=1008 m3
mSO2 tạo ra=1920 kg
Giải thích các bước giải:
\[\begin{array}{l}
4Fe{S_2} + 11{O_2} \to 2F{e_2}{O_3} + 8S{O_2}\\
4FeS + 7{O_2} \to 2F{e_2}{O_3} + 4S{O_2}
\end{array}\]
Ta có
mFeS2=2,08x57,7%=1,2 tân=1200 kg
mFeS=2,08-1,2=0,88 tấn=880 kg
ta có
đốt cháy 120 gFeS2 cần dùng 61,6 l O2 và tạo 128 g SO2
1200 kg x m3 y kg
=>x=616 m3 y=1280 kg
đốt cháy 88 gFeS2 cần dùng 39,2l O2 và tạo 64g SO2
880 kg a m3 b kg
=>a=392 m3 y=640 kg
=>VO2 cần=616+392=1008 m3
mSO2 tạo ra=640+1280=1920 kg
Hãy giúp mọi người biết câu trả lời này thế nào?
Đáp án:
Giải thích các bước giải:
có 2,08 tấn = 2,08 .$10^{6}$ gam
có mFeS2 = $\frac{2,08.10^{6}.57,7}{100}$ = 1,2.$10^{6} gam
⇒ nFeS2 = $\frac{1,2.10^{6}}{120}$ = 0,01.$10^{6}$ mol
có mFeS = 2,08.$10^{6}$ - 1,2.$10.^{6}$ = 0,88.$10^{6}$ gam
⇒ nFeS = $\frac{0,88.10^{6}}{88}$ = 0,01.$10^{6}$ mol
PTHH :
4FeS2 + 11O2 --to--> 2Fe2O3 + 8SO2
4FeS + 57O2 --to--> 2Fe2O3 + 4SO2
Theo PT , có : nO2 = 11/4 . nFeS2 + 7/4 . nFeS = 0,045.$10^{6}$ mol
⇒ V O2 = 0,045.$10^{6}$ .22,4 = 1008000 lít = 1008 m³
Theo PT , có : nSO2 = 2nFeS2 + nFeS = 0,03.$10^{6}$ mol
⇒ mSO2 = 0,03.$10^{6}$ .64 = 1920000 gam = 1,92 tấn
Hãy giúp mọi người biết câu trả lời này thế nào?
Bạn muốn hỏi điều gì?
Bảng tin
Bạn muốn hỏi điều gì?
 Inbox: m.me/hoidap247online
Inbox: m.me/hoidap247online Trụ sở: Tầng 7, Tòa Intracom, số 82 Dịch Vọng Hậu, Cầu Giấy, Hà Nội.
Trụ sở: Tầng 7, Tòa Intracom, số 82 Dịch Vọng Hậu, Cầu Giấy, Hà Nội.