Hãy luôn nhớ cảm ơn và vote 5*
nếu câu trả lời hữu ích nhé!
TRẢ LỜI
- diemhuongsphh

Đây là câu trả lời đã được xác thực
Câu trả lời được xác thực chứa thông tin chính xác và đáng tin cậy, được xác nhận hoặc trả lời bởi các chuyên gia, giáo viên hàng đầu của chúng tôi.
Đáp án:
D. a = 5
Giải thích các bước giải:
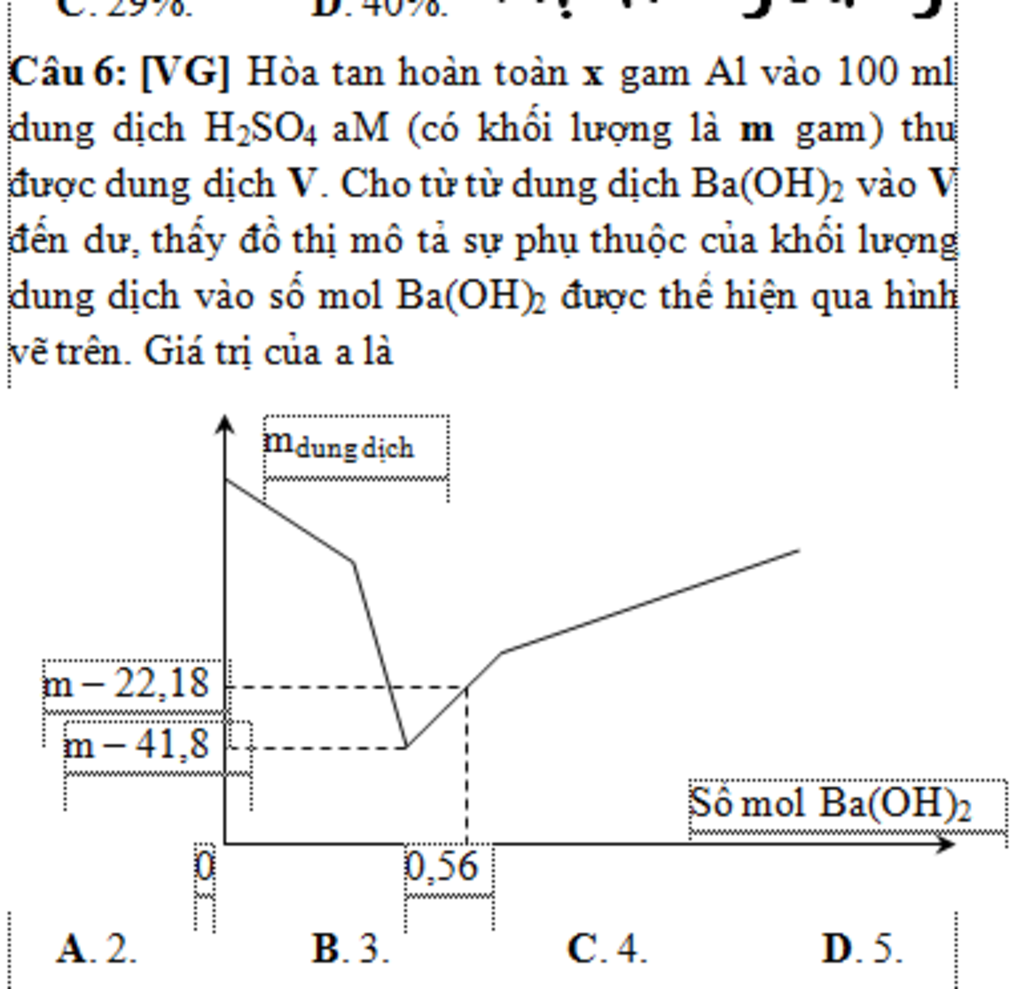
Nhìn vào đồ thị ta thấy, tại giai đoạn 1: m dung dịch giảm ít hơn so với giai đoạn 2. Vậy chứng tỏ trong dung dịch V có chứa $Al_2(SO_4)_3;\ H_2SO_4$
Tới giai đoạn 3, m dung dịch tăng dần lên do $Al(OH)_3$ bị hòa tan.
Giai đoạn 4, m dung dịch cứ thế tăng lên do $Ba(OH)_2$ tiếp tục được cho vào.
Các PTHH xảy ra:
$2Al+3H_2SO_4→Al_2(SO_4)_3+3H_2↑$ (1)
$H_2SO_4+Ba(OH)_2→BaSO_4↓+2H2O$ (2)
$Al_2(SO_4)_3+3Ba(OH)_2→3BaSO_4↓+2Al(OH)_3↓$ (3)
$2Al(OH)_3+Ba(OH)_2→Ba(AlO_2)_2+4H_2O$ (4)
+) Xét tại điểm cuối của giai đoạn 2 (điểm tương ứng với $m_{dd} = m-41,8$)
Tại đây xảy ra PT số (1), (2), (3). PƯ số (3) xảy ra vừa đủ.
Gọi số mol của $Al_2(SO_4)_3;\ H_2SO_4$ lần lượt là a, b mol
Ta có: m - 41,8 ⇒ Khối lượng dung dịch của $H_2SO_4$ bị giảm 41,8g
$⇒ Δm_{\text{giảm}}=m_{Al}+m_{Ba(OH)_2(2),(3)}-m_{H_2}-m_{BaSO_4(2),(3)}-m_{Al(OH)_3(3)}$
$⇒-41,8=27.(2a)+171.(3a+b)-2.(3a)-233.(b+3a)-78.(2a)$
$⇒294a+62b=41,8$ (5)
+) Xét tại điểm (0,56; m-22,18)
Tại đây xảy ra thêm phản ứng số (4), Gọi $n_{Ba(OH)_2(4)}=z\ mol$
Ta có:
$⇒ Δm_{\text{giảm}}=m_{Al}+m_{Ba(OH)_2(2),(3),(4)}-m_{H_2}-m_{BaSO_4(2),(3)}-m_{Al(OH)_3(3)-(4)}$
$⇒-22,18=27.(2a)+171.(3a+b+z)-2.(3a)-233.(b+3a)-78.(2a-2z)$ (6)
Lấy (6) - (5): $-22,18-(-41,18)=171z+2.78z⇒z=0,06$
$⇒n_{Ba(OH)_2(2),(3)}=3a+b=0,56-0,06=0,5$ (7)
Giải hệ PT (5), (7) $⇒ a=0,1;\ b=0,2$
Vậy $n_{H_2SO_4}\text{tổng}=3.0,1+0,2=0,5\ mol$
$⇒C_M{H_2SO_4}=\dfrac{n}{V}=5\ M$
Hãy giúp mọi người biết câu trả lời này thế nào?
Bạn muốn hỏi điều gì?
Bảng tin
Bạn muốn hỏi điều gì?
 Inbox: m.me/hoidap247online
Inbox: m.me/hoidap247online Trụ sở: Tầng 7, Tòa Intracom, số 82 Dịch Vọng Hậu, Cầu Giấy, Hà Nội.
Trụ sở: Tầng 7, Tòa Intracom, số 82 Dịch Vọng Hậu, Cầu Giấy, Hà Nội.